Nature Methods 如此评价类器官(Organoids)技术:利用干细胞直接诱导生成三维组织模型,为人类生物学研究提供了强大的方法,目前对于这种工具的研究正在不断发展进步中。

生命(至少)是在三维空间中发生并存在的,利用在培养皿中形成的平层细胞开展生命的分子细胞学研究具有很大的局限性,无法揭示生物学的全部事实。类器官技术也是在这一背景下应运而生。
这项技术始于2009年,荷兰Hubrecht研究所的Clevers团队成功的将成体干细胞培养成为小肠的隐窝和绒毛结构。
2011年,该领域再次获得突破,日本RIKEN发育生物学中心的研究人员将胚胎干细胞构建成为视杯结构。
2013年,来自日本、德国、美国的科研人员分别构建出肝芽、迷你肾和微型大脑,使该领域获得了国际的广泛关注,并被Science评选为2013年的十大突破。
近年来,该技术不仅在更多种类的组织器官构建中获得了突破,在疾病研究、药物筛选、药物毒理测试等领域也展现出作为组织模型的应用潜力。此次,Nature Methods将其确定为2017年的年度技术,再次凸显了该技术的巨大发展潜力,未来该领域有望引起全球更大范围的研究热潮。
1
干细胞—胃底类器官
2017年1月4日,美国辛辛那提儿童医院医疗中心的研究人员成功利用人类多能干细胞培育出能产生胃酸和消化酶的胃底类器官。研究人员发现了在小鼠胚胎中调控胃细胞发育的重要信号通路Wnt/β-catenin,并通过在人类多能干细胞(hPSC)来源的前肠祖细胞中激活该通路,实现了人类胃底类器官(hFGOs)的构建。同时,利用hFGO,研究人员还识别出调控表皮形态发生及胃底主细胞和壁细胞分化的关键分子信号。
相关研究以Wnt/β-catenin promotes gastric fundus specification in mice and humans为题发表在Nature上。
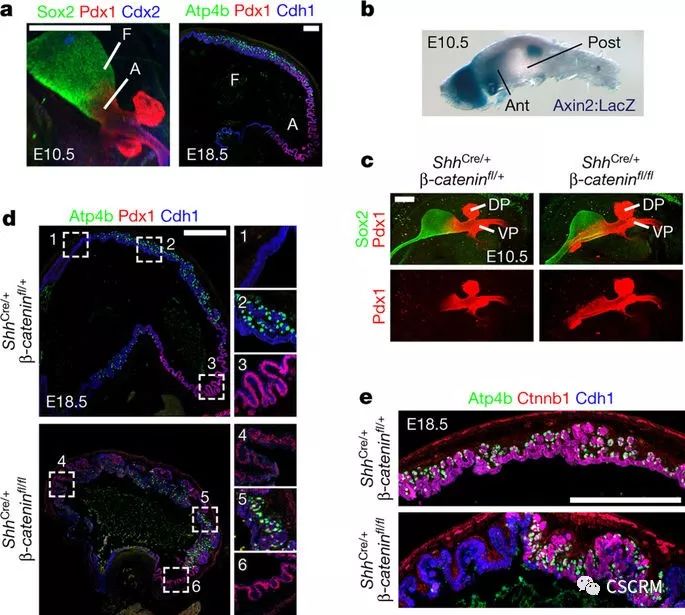
(图片来源:Nature, doi: 10.1038/nature21021)
2
干细胞—功能性肠道类器官
2017年1月12日,日本国立成育医疗研究中心的研究人员利用人类多能干细胞培育出功能性肠类器官。该肠类器官含有源自3个胚层的肠细胞:肠上皮细胞、杯状细胞、潘氏细胞和肠内分泌细胞,并具有肠道功能,包括肽的吸收,以及响应组胺和抗胆碱能药物的刺激而表现出肠蠕动。
相关研究以A xenogeneic-free system generating functional human gut organoids from pluripotent stem cells为题发表在JCI Insight上。
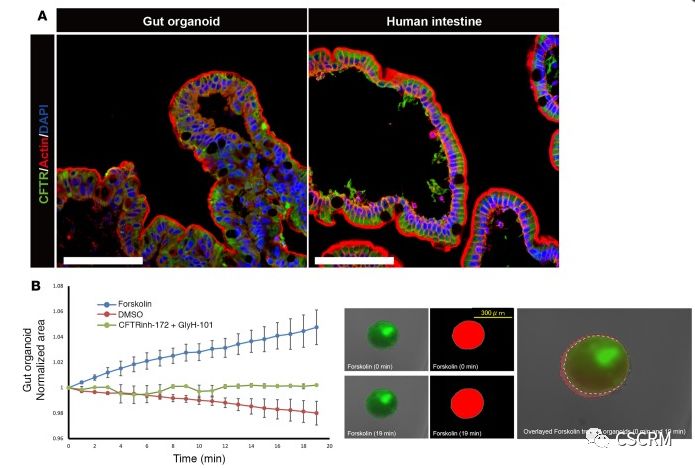
(图片来源:JCI Insight, doi: 10.1172/jci.insight.86492)
3
干细胞—角膜类器官
2017年1月27日,美国约翰•霍普金斯大学医学院的研究人员利用人类诱导多能干细胞成功培养出角膜类器官。该角膜类器官具有与正常发育的角膜同样的特征,包含三种不同的细胞类型:上皮细胞、基质细胞和内皮细胞。
相关研究以Cornea organoids from humaninduced pluripotent stem cells为题发表在Scientific Reports上。
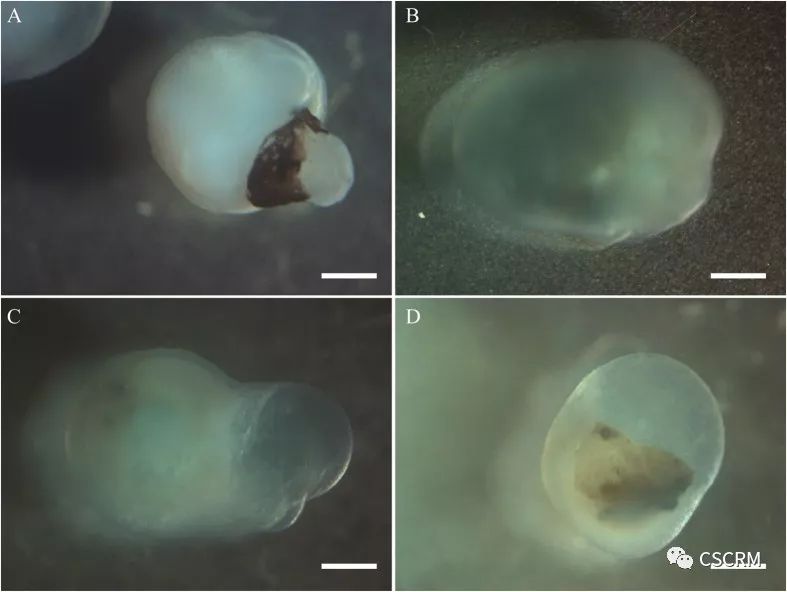
(图片来源:Scientific Reports, doi: 10.1038/srep41286)
4
干细胞—肺脏类器官
2017年4月24日,美国哥伦比亚大学医学中心的研究人员利用人多能干细胞生成了模拟肺部结构和功能的类器官,包含分支气道和肺泡结构,且该分支结构达到了人类妊娠中期的发育水平。为了验证其功能,科研人员利用引发婴幼儿小气道阻塞和细支气管炎的呼吸道合胞体病毒(RSV)在体外对其进行感染,发现会导致被感染细胞肿胀,并分离、脱落到类器官腔,与人类肺部观察到的现象一致。此外,研究人员在类器官中引入了引起早发型肺纤维化的HPS1突变,发现能够导致细胞外基质和间充质细胞的积聚,表明类器官具有体外重建肺纤维化疾病模型的潜力。
相关研究以A three-dimensional model ofhuman lung development and disease from pluripotent stem cells为题发表在Nature Cell Biology上。
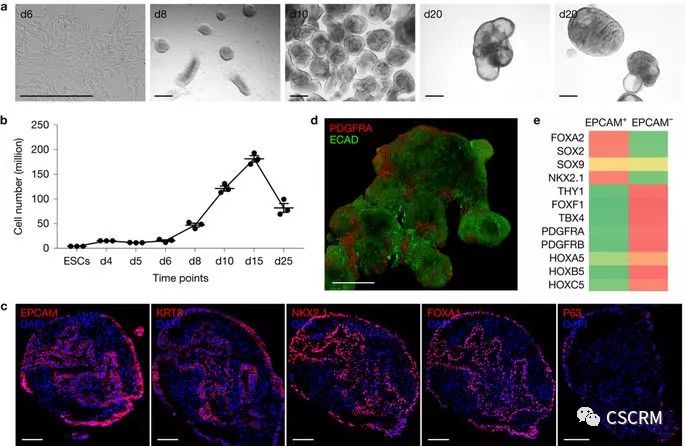
(图片来源:Nature Cell Biology, doi: 10.1038/ncb3510)
5
干细胞—结肠类器官
2017年6月19日,美国威尔康奈尔医学院(Weill Cornell Medicine College)的研究人员利用家族性腺瘤性息肉病(FAP)患者皮肤成纤维细胞的诱导多能干细胞构建了结肠类器官。研究证实,构建的结肠类器官具有结肠组织的生物学特征,包含干细胞、短期扩增细胞、分化细胞等。研究人员进一步利用构建的结肠类器官进行了XAV939、雷帕霉素、遗传霉素三种药物的体外测试,证实了其在结直肠癌靶向药物开发中的应用潜力。
相关研究以Colonic organoids derived from human induced pluripotent stem cells for modeling colorectal cancer and drug testing为题发表在Nature Medicine上。
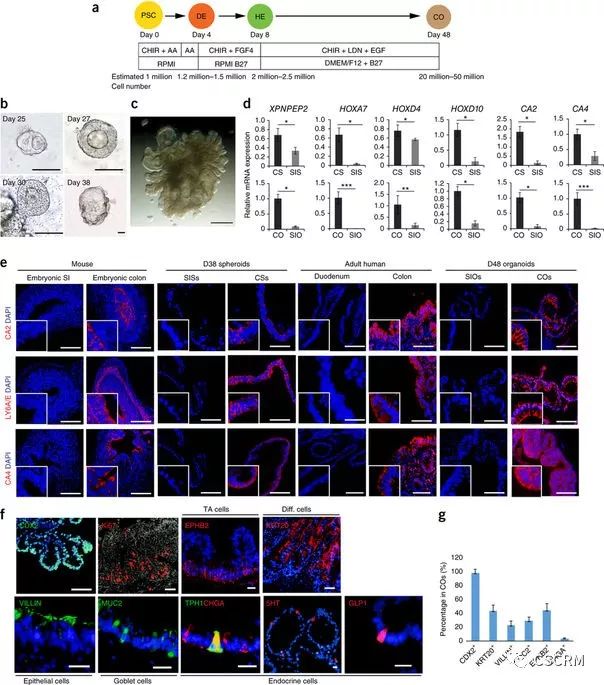
(图片来源:Nature Medicine, doi: 10.1038/nm.4355)
6
干细胞—结肠类器官
2017年7月6日,美国辛辛那提儿童医院的研究人员利用人类多能干细胞培育出结肠类器官。研究人员基于动物模型展开分子和遗传学筛查,并结合多个数据库,发现BMP信号对肠上皮细胞发挥调控作用。通过短暂激活BMP信号,成功促使干细胞发育形成结肠类器官(HCO)。进一步研究发现,移植到实验鼠体内发育6到10周后,这一类器官的形态、结构、分子和细胞特性等都与人类结肠相似。
相关研究以Differentiation of human pluripotent stem cells into colonic organoids via transient activation of BMP signaling为题发表在Cell Stem Cell上。
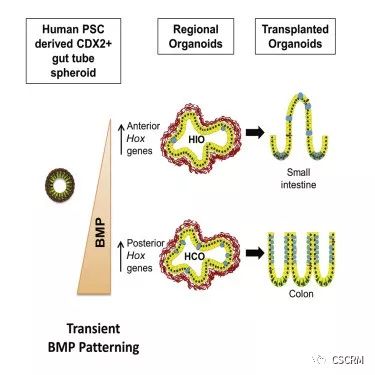
(图片来源:Cell Stem Cell, doi: 10.1016/j.stem.2017.05.020)
7
干细胞—结肠类器官
2017年10月13日,荷兰乌得勒支大学的研究人员利用CRISPR-Cas9技术敲除了人类结肠类器官中的关键DNA修复基因,并进行延迟亚克隆(delayed sub-cloning)和全基因组测序,准确地模拟了错配修复缺陷型结直肠癌中观察到的突变,为癌症突变研究提供了有效的工具。
相关研究以Use of CRISPR-modified human stem cell organoids to study the origin of mutational signatures in cancer为题发表在Science上。
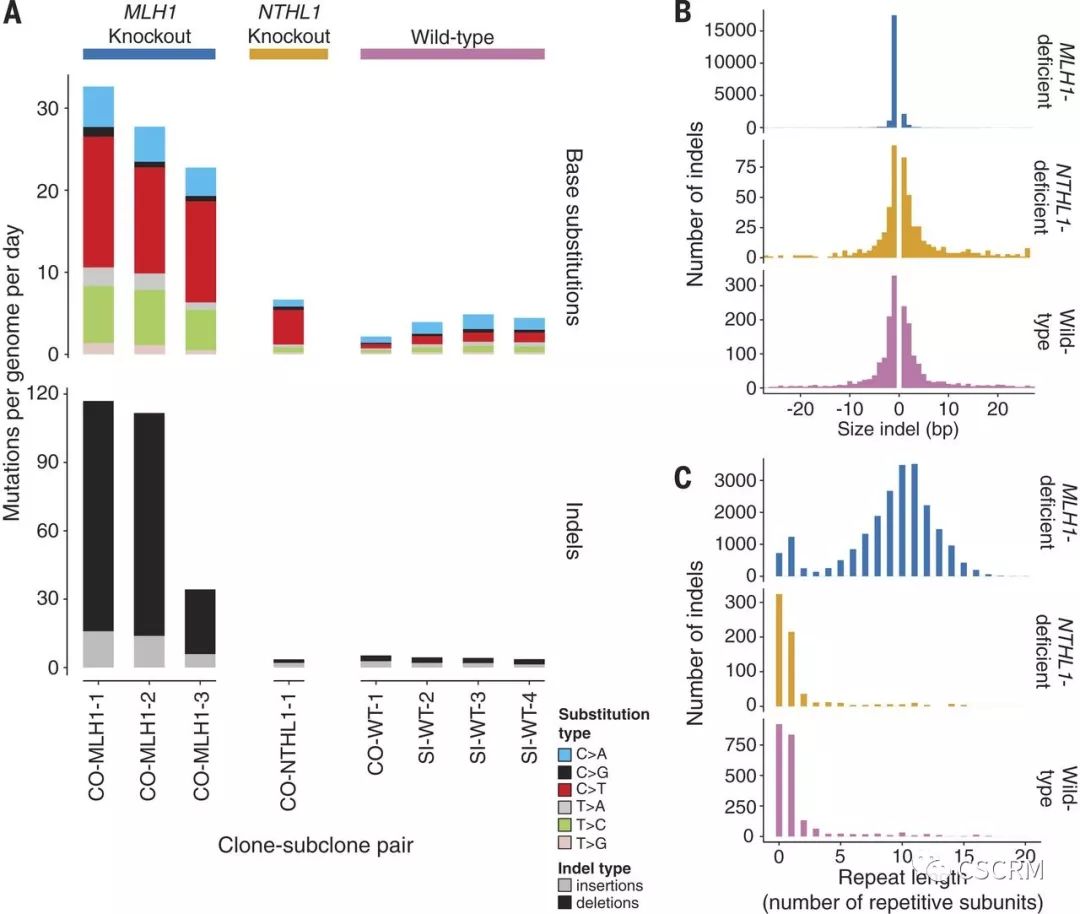
(图片来源:Science, doi: 10.1126/science.aao3130)
参考文献:
[1] McCracken K W, Aihara E, Martin B, et al. Wnt/β-catenin promotes gastricfundus specification in mice and humans[J]. Nature, 2017, 541(7636): 182-187.
[2] Uchida H, Machida M, Miura T, et al. Axenogeneic-free system generating functional human gut organoids from pluripotentstem cells[J]. JCI Insight, 2017, 2(1): e86492.
[3] Foster J W, Wahlin K, Adams S M,et al. Cornea organoids from humaninduced pluripotent stem cells[J]. Scientific Reports, 2017, 7: 41286.
[4] Chen Y W, Huang S X, et al. A three-dimensional model of humanlung development and disease from pluripotent stem cells[J]. Nature Cell Biology, 2017, 19(5): 542-549.
[5] Crespo M, Vilar E, Tsai SY, et al. Colonic organoids derived from human induced pluripotent stem cells formodeling colorectal cancer and drug testing[J]. Nature Medicine, 2017, 23(7):878-884.
[6] Múnera J O, Sundaram N, Rankin SA, et al. Differentiation of human pluripotent stem cells into colonicorganoids via transient activation of BMP signaling[J]. Cell Stem Cell, 2017, 21(1): 51-64.
[7] Drost J, VanBoxtel R, Blokzijl F, et al. Use of CRISPR-modified human stemcell organoids to study the origin of mutational signatures in cancer[J]. Science, 2017, 358(6360): 234-238.
复制本文链接 文章为作者独立观点不代表本网站立场,未经允许不得转载。

 京公网安备
11010802036058号
京公网安备
11010802036058号
评论